Día a día aumenta el número de enfermedades en cuya
etiología estaría involucrado el estrés oxidativo que se produce cuando el
ataque oxidativo supera las defensas antioxidantes. El tejido nervioso parece
ser un blanco propicio para los compuestos prooxidantes, dada sus características
químicas, tales como alto contenido en ácidos grasos poliinsaturados, altas
concentraciones de hierro y bajo contenido en enzimas antioxidantes. Hay
investigaciones que demuestran una clara intervención del estrés oxidativo en
el desarrollo de la enfermedad de Alzheimer, en Parkinson y en esclerosis
lateral amiotrófica, entre otras enfermedades del sistema nervioso.
También se ha encontrado asociación entre estrés y
envejecimiento y con numerosas enfermedades adquiridas por exposición a xenobióticos.
Muchas investigaciones en marcha están tratando de explicar la participación
de las especies reactivas de
oxígeno (EROs) en el desarrollo y características clínicas de varias
enfermedades, tales como diabetes, cirrosis alcohólica, hipertiroidismo, cáncer,
etc. De los resultados obtenidos se trata de sugerir o encontrar nuevas
estrategias para el tratamiento de estas enfermedades y/o recomendar el uso de
antioxidantes como medicina preventiva o adicional al tratamiento específico de
las mismas.
Por último, hay fuerte interés en conocer la asociación
entre estrés oxidativo y actividad física. Varios trabajos demuestran que
existe inducción de estrés oxidativo en individuos sujetos a intensa
ejercitación física, pero al mismo tiempo se ha comprobado que en estos
individuos aumentan las defensas antioxidantes tanto enzimáticas como mediadas
por atrapantes de radicales libres de bajo peso molecular. Por otra parte, se ha
comprobado que la actividad física conlleva una variación en la naturaleza de
las lipoproteínas plasmáticas, favoreciendo el contenido del llamado
colesterol bueno frente al malo, con la consiguiente disminución de riesgo
coronario. Hay varios trabajos que demuestran la implicancia de la peroxidación
lipídica de las fracciones proaterogénicas en el desarrollo de la
aterosclerosis, la cual podría prevenirse, por lo tanto, mediante un adecuado
entrenamiento físico.
El estrés oxidativo
El
estrés oxidativo es un estado de la célula en la cual se encuentra alterada la
homeostasis óxido-reducción intracelular, es decir el balance entre
prooxidantes y antioxidantes. Este desbalance se produce a causa de una excesiva
producción de especies reactivas de oxígeno (EROs) y/o por deficiencia en los
mecanismos antioxidantes, conduciendo a daño celular.
En analogía al término
“estrés oxidativo”, Hausladen y Stambler han denominado “estrés
nitrosativo” a la excesiva o desregulada formación del radical óxido nítrico
(NO.) y especies reactivas del Nitrógeno (ERNs) derivadas del mismo
(1).
Estado de óxido - reducción de la célula.
El estado de óxido - reducción
de la célula está determinado por el equilibrio entre las contrapartes
oxidadas y reducidas de los distintos compuestos biológicos presentes en ella,
principalmente de aquellos que se encuentran en mayor proporción. El tripéptido
glutation (GSH, g-L-glutamil-L-cisteinil-glicina),
debido a su alta concentración intracelular (5-10 mM), se considera un
regulador homeostático del estado de óxido- reducción celular. Este
metabolito se encuentra presente en su forma oxidada en sólo un 1 % del total,
es decir que predomina ampliamente su forma reducida (GSH) sobre la oxidada
(GSSG). Esto trae como consecuencia que un ligero desplazamiento del equilibrio
hacia la forma oxidada afecta drásticamente el estado de óxido-reducción
general, debido a su participación en muchos equilibrios de óxido reducción
acoplados. En particular esto es crítico para la regulación (prendido o apagado) de
algunos factores de transcripción , cuya actividad depende del estado de óxido-reducción
en el que se encuentren. El siguiente esquema representa los procesos que pueden
ocurrir, relacionados al prendido y apagado de genes, bajo condiciones de estrés
(-S* grupo sulfhidrilo modificado):
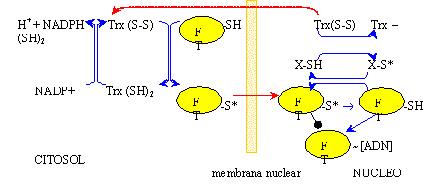
Cuando un grupo -SH crítico
sufre una modificación oxidativa la proteína afectada puede perder su
funcionalidad. La siguiente serie de reacciones muestra los distintos equilibrio
en los que puede participar un residuo cisteína:
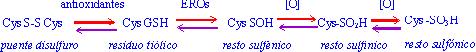
Especies
reactivas del Oxígeno (EROs)
Las principales especies
reactivas del Oxígeno son: el radical superóxido (O2-.),
el peróxido de Hidrógeno (H2O2) y el radical oxidrilo
(HO.). Una de las
principales fuentes de EROs es la cadena respiratoria, donde pueden ocurrir las
siguientes transferencias de electrones:
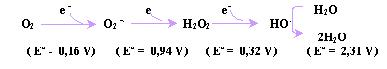
En
ella aproximadamente un 3 % de los electrones provenientes de NADH, por la
incompleta reducción del Oxígeno, se desvían hacia la formación de EROs. Las
EROs son capaces de oxidar macromoléculas biológicas, tales como proteínas, lípidos
y ácidos nucleicos (2-4). Por otra parte, el H2O2 puede
reaccionar con metales divalentes (libres o unidos a proteínas) y producir HO.,
vía reacción de Fenton. El ejemplo tipo es la reacción con Fe++
libre, que ocurre según la siguiente reacción:
En
forma similar, puede reaccionar también con el grupo prostético de metaloproteínas
conteniendo hierro (ej. con la dihidroxiácido dehidrasa, la 6 fosfogluconato
dehidrasa, las fumarasas A y B o la aconitasa), según la
reacción
de Haber Weis:
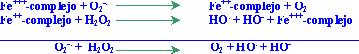
El HO. puede reaccionar con distintas macromoléculas (proteínas,
lípidos y ácidos nucleicos, principalmente), en las que por cesión de un
electrón produce otras especies reactivas, a través de mecanismos y de
intermediarios aun desconocidos. En estos casos se dice que ha intervenido el
radical oxidrilo, entendiendo como tal a un radical proveniente de oxidaciones
univalentes, iniciadas por una reacción de tipo Fenton (5). En este tipo de
reacciones la hidroxilación y la abstracción de Hidrógeno son las
modificaciones más comunes que sufre el sustrato orgánico involucrado y se
generan otros radicales libres orgánicos tales como: los radicales alcohoxilos
(RO.), peroxilos (ROO.) y sulfoderivados.
La formación de
radical superóxido ( O2.- ) también puede ocurrir a
nivel de la NADPH-oxidasa según la siguiente reacción:
2O2
+ NADPH ® 2O2 .-
+
NADP+ + H+
con la participación de un
complejo de proteínas, que por estrés oxidativo sufren modificaciones
conformacionales, exponiendo distintos sitios de interacción proteica, que le
permiten unirse a 2 ferro-proteínas integrales de membrana. De esta manera
queda formado un complejo proteico con actividad NADPH-oxidasa (6). La activación
de este complejo está mediada por el sistema Ras.
Las
proteínas Ras forman parte de una superfamilia de proteínas con afinidad por
GTP (7). Cuando Ras se une a GTP, se activa su actividad GTPasa, se hidroliza un
fosfato, Ras pierde afinidad por el nucleótido resultante (GDP), y luego por
GAP (la proteína activante de su actividad GTPasa). La energía liberada
durante este ciclo se usa para producir modificaciones conformacionales en
distintos sistemas proteicos, que conducen a la activación de complejos enzimáticos.
Un ejemplo de este complejo mecanismo es la activación de la NADPH oxidasa
arriba mencionada, la cual se ha comprobado que, bajo condiciones de estrés
oxidativo provocado por invasión por patógenos, se activa a través de un
mecanismo regulado por Ras. En un medio aeróbico se desarrollarán las
siguientes reacciones:

Existen
otras dos EROs, con características especiales: el Oxígeno singulete (1O2)
y el hipoclorito (en su forma no protonada ClO- o protonada, llamado
también ácido hidrocloroso).
El 1O2 es una forma excitada de la molécula de Oxígeno
diatómico (triplete):
94,3 kJ/mol
O2
+ ®
1O2
Esta
especie reactiva tiene gran tendencia a reaccionar con moléculas orgánicas ya
que, al tener un momento de espín igual a cero, comparte con éstas el estado
singulete. El 1O2 puede originarse por transferencia de
energía desde otra molécula reactiva, por reacciones fotoquímicas o por
reacciones en ausencia de Oxígeno. Las siguientes ecuaciones representan su
formación en esta última situación, que ocurre especialmente en neutrófilos,
ricos en cloroperoxidasas (que aceleran la primera reacción) y en H2O2
(el cosustrato en la segunda
reacción):
H2O2
+ Cl- ® OCl- + H2O
H2O2
+ OCl- ®
1O2 + H2O + Cl-
La producción fotoquímica de
1O2, puede ocurrir a partir de fotosensibilizadores endógenos
(porfirinas, flavinas, quinonas) o exógenos (Rosa de Bengala, Azul de Metileno)
y por radiación visible o UV. También puede generarse en procesos
inflamatorios o por excitación química con carbonilos excitados, proceso que
puede ocurrir aun en oscuridad. La irradiación tópica de tejidos tumorales
preexpuestos a sensibilizadores, lleva a la necrosis por producción fotodinámica
fundamentalmente del 1O2
(8).
Efectos
de las EROs
Se ha demostrado que el 1O2
es un mediador de los efectos
citotóxicos inducidos por la radiación UVA, produciendo activación del factor
de transcripción AP-2, activa la cascada de señales que involucra otros
factores de la cascada de señales tales como las
quinasas de la región N terminal de c-Jun (JNK, p38-MAPK y NF-kB), participando en el sistema de transducción de señales, que
lleva a apoptosis o a recuperación de la célula , dependiendo del estado
inicial de la misma. Entre los daños a macromoléculas que puede ejercer el 1O2
, está el daño al ADN, debido a la oxidación de residuos guanina a
7-hidro-8-oxo deoxignanosina (8 oxo-Gu). Este nucleótido lleva luego a la
transversión de G:C a T:A, provocando así mutaciones que pueden llevar a la
muerte celular.
Las proteínas cuya traducción
se ha reportado que es inducida por 1O2 son, entre otras:
la hemooxigenasa 1 (HO-1), la colagenasa instersticial (metaloproteinasa 1, de
la matriz o MMP-1), las interleuquinas IL-1
a/b
e IL-6, la molécula de adhesión intercelular ICAM-1 y el ligando Fas.
La HO (que se induce también
por radiación UVA y por H2O2 y está modulada por niveles
de GSH) cataliza la primera de las siguientes reacciones, que llevan a la
producción de dos especies antioxidantes, la bilirrubina y la biliverdina:
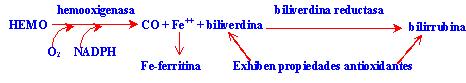
El átomo de Fe que se libera
en la conversión del hemo a biliverdina, se transporta a la médula ósea por
medio de una b- globina, llamada
transferrina, por lo que la mayor parte de este Fe se recupera en lugar de
excretarse. Una parte pasa, en el hígado, a la ferritina, almacenándose en un
hueco de aproximadamente 12 mm de diámetro, donde se pueden alojar cerca de
4000 iones férricos/molécula de enzima. Es evidente que la cantidad de hierro
libre en la célula es muy baja, constituyendo estas proteínas (la ferritina y
la transferrina) un importante mecanismo de defensa antioxidante, ya que al
secuestrar al hierro impiden que participe en la reacción de Fenton y se inicie
la cadena de radicales libres arriba comentada.
Respuesta
adaptativa al estrés oxidativo
Se ha comprobado que el
promotor de la hemooxigenasa 1 (HO-1) contiene sitios de unión a factores de
transcripción AP-1, AP-2 y NF-kB, que
también se activan por estrés oxidativo, resultando en la síntesis de
numerosas proteínas, que se conocen como enzimas respondedoras al estrés. La
inducción de la HO-1 se considera una “respuesta adaptativa” al estrés
oxidativo. La respuesta adaptativa u hortesis es el fenómeno celular por el
cual la exposición a un agente tóxico (en concentraciones subletales) provoca
una respuesta celular que protejerá posteriormente a la célula contra los
efectos deletereos del mismo tóxico a concentraciones letales, dicho en otras
palabras, es un efecto benéfico desencadenado con bajo nivel de exposición a
un agente que es dañino a altos niveles. Este efecto es muy importante en casos
de estrés oxidativo. Así, se ha comprobado que la exposición a bajos niveles
de radiación o a O2 hiperbárico aumenta las defensas antioxidantes.
La terapia con O2 hiperbárico al hombre (100% O2 a 2,5
atmósferas), por ejemplo, induce cambios significativos en el daño oxidativo
al ADN, en células sanguíneas periféricas, pero luego el daño se estabiliza,
en tanto que las defensas antioxidantes suben.
El resultado es una bajada en la línea de base del daño celular total,
específicamente a nivel de daño oxidativo al ADN, desencadenado inicialmente
por el tratamiento. Pretratamientos de este tipo se suelen utilizar en pacientes
que deben ser sometidos a una intervención quirúrgica, para minimizar los daños
laterales provocados por el estrés oxidativo. Por otra parte (9), se ha
comprobado que con tratamientos que provocan bajos niveles de oxidación y en
condición normales de reparación, las células toleran cierta carga de aductos
oxidados que contribuyen a la velocidad de mutación espontánea y muerte de células
extremadamente dañadas, lo cual puede resultar benéfico para el sistema total
(órgano y/o tejido) bajo determinadas condiciones.
Otras fuentes de EROs
Otra fuente de EROs está relacionada a la cupla
xantino/xantino oxidasa (oxidasas catabólicas, presentes en los peroxisomas)
(10). La acumulación de hipoxantina y xantina, bajo condiciones anaeróbicas,
de isquémia/reperfusión (deficiencia en la irrigación sanguínea -que
empobrece la llegada de sangre y, por consiguiente, de Oxígeno a un tejido- con
posterior reflujo sanguíneo y consecuente afluencia de Oxígeno) o de bajo
contenido energético, puede desembocar en la producción de EROS,
según la siguiente cascada de reacciones:
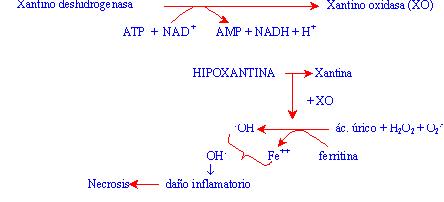
Especies
reactivas del Nitrógeno (ERNs)
Las principales ERNs son el óxido
nítrico (NO.) y el
peroxinitrito (ONOO-.)
considerado como uno de los más potentes oxidantes biológicos (11). Las ERNs
pueden dañar y matar células por distintos mecanismos: inactivación de los
distintos complejos de la cadena respiratoria (12), daño a proteínas y a lípidos
(3, 4, 13, 14), inhibición de síntesis proteica o de ADN (15, 16), depleción
de GSH o de ATP (17, 18).
El ONOO-
está en equilibrio con una forma activada de estructura desconocida, que
reacciona con metionina para dar metilsulfóxido o, en presencia de CO2,
un derivado con actividad nitrante de compuestos aromáticos (3). La
principal fuente de ERNs, en células de mamíferos, es la oxidación enzimática
de L-arginina por la NO sintasa (19).
El NO. es una molécula de señal ubicua, que funciona en la
regulación de distintos procesos en los sistemas nervioso, cardiovascular e
inmune (20, 21). Está asociado a procesos inflamatorios neurotóxicos y de
isquemia/reperfusión. Se ha propuesto que el NO. actuaría induciendo la producción mitocondrial de
peroxinitrito. Este produciría a su vez la inhibición del complejo I de la
cadena respiratoria (NADH:Ubiquinona reductasa), lo cual tiene un efecto crítico
sobre el suplemento de energía en varios tejidos (22) y sobre la producción de
EROs. Los efectos del NO.
sobre la generación de EROs mitocondrial son complejos (11), la producción de
EROs y ERNs inducida por NO y su posterior modulación son iniciados por la
reacción entre NO y el ubiquinol llevando a la formación y autooxidación de
la ubisemiquinona. Posteriormente se forma una intrincada red de equilibrios de
óxido-reducción, involucrando al ubiquinol, al anión superóxido, al
peroxinitrito y al óxido nítrico, que cubre un amplio campo en los aspectos
regulatorios y protectores contra el estrés oxidativo. El balance final de daño
por estrés oxidativo o de protección por defensas antioxidantes en
mitocondrias, dependerá del contenido de ubiquinol y de NO en el estado
estacionario, del nivel de enzimas antioxidantes y de la extensión de la
inhibición inducida en el Complejo I en la membrana mitocondrial.
Otro tipo de especies reactivas que se pueden producir durante procesos
de estrés oxidativo, son las llamadas especies bioluminiscentes (BLUE) de larga
vida (23). En nuestro laboratorio, en estudios experimentales de alcoholismo crónico
y de intoxicación crónica con hidrocarburos aromáticos polihalogenados,
pudimos comprobar que se generan estas BLUE, cuya detección permite hacer un
seguimiento de la evolución de las patologías asociadas (24). El hecho que
ambos tratamientos producen especies reactivas (24, 25)
avalan la hipótesis que las BLUE provendrían del estrés oxidativo
desencadenado por este tipo de tratamientos.
Defensas antioxidantes
Si bien todos los organismos
vivos soportan numerosos factores endógenos y exógenos de estrés oxidativo,
al mismo tiempo poseen numerosos sistemas de defensas antioxidantes regulables,
enzimáticos y no enzimáticos.
Existen
enzimas que actúan específicamente sobre determinadas especies reactivas (5).
Así, la superóxido dismutasa dismuta (reacción a través de la cual dos moléculas
iguales se transforman en otras dos moléculas distintas) al O2-.
a O2 y H2O2, la catalasa transforma al H2O2
en O2 y agua, la GSH–peroxidasa cataliza la reducción de peróxidos
(ROOH, inclusive al H2O2) a alcoholes (ROH), aprovechando
el potencial reductor del GSH. Existen otras enzimas, tales como las quinonas
reductasas y hemo oxigenasa, que pueden prevenir la formación de EROs, por
ciclado de electrones.
La familia de las superóxido
dismutasas (SOD) ha ido en aumento y ya se han descubierto al menos tres
miembros además de las dos proteínas inicialmente detectadas (la Mn SOD
mitocondrial y la Zn/ Cu- SOD citoplasmática, que dan cuenta del 100% de la
actividad SOD intracelular) (5). La Cu/ Zn- SOD citosólica, es inhibible por
cianuro, su actividad representa el 90% de la actividad del homogenato total. La
Mn- SOD, mitocondrial se puede determinar por diferencia entre la actividad SOD
total y la actividad SOD en presencia de cianuro. Se han descubierto dos SOD
extracelulares: la llamada EC- SOD extracelular, en humanos se presenta como un
homotetrámero siendo secretada por las células que la producen. También ha
sido detectada en plantas, bacterias y en nemátodos. Su función sería
interceptar el O2.- exógeno (por ejemplo, los liberados
por leucositos fagocíticos) evitando de esta forma la posible reacción del NO,
con el O2.-, aumenta la vida del NO y disminuye la
generación del ONOO-, uno de los oxidantes más potentes. Está
glicosilada y exhibe afinidad por polisacáridos sulfatados, tales como la
heparina o la heparina sulfatos, por esta razón, si bien se detecta en plasma
sanguíneo se encuentra unida a la matriz extracelular. La segunda SOD
extracelular, el Cu/Zn-SODp o
periplásmica, existe en unas pocas especies de bacterias Gram negativas. Su
función sería proteger a la célula contra el O2.- exógeno.
La última SOD descripta es una Ni-SOD, detectada en Streptomyces, es homotetramérica
y no tiene homología con las SOD previamente reportadas.
Regulación
de la respuesta al estrés oxidativo
El gen de las SOD,
conjuntamente con el de otras proteínas sensibles al estrés está regulado por
el regulón SoxRS. Un regulón es un grupo de genes regulados coordinadamente.
En el caso del regulón SoxRS, el factor activante es el aumento en la
concentración del O2.-. Algunos de los productos
resultantes al activarse SoxRS son: la Mn –SOD (enzima encargada de eliminar
O2.-), la Glu 6p deshidrogenasa
(que asegura el suplemento de NADPH), la endonucleasa IV (miembro del
sistema de reparación del ADN dañado), la ferredoxina reductasa (que activa
las Fe-S proteínas, reparando su centro 4Fe-4S, dañado por el estrés
oxidativo), la mic F (disminuye la porosidad de la membrana mitocondrial
interna, ayudando así a recomponer el potencial de membrana). El péptido SoxR,
es el sensor de óxido-reducción, que en su estado oxidado activa a la proteína
SoxS. La SoxS activa vuelve a unirse al regulón SoxRS, activando su operón y
causando la activación transcripcional. El regulón SoxRS representa la mitad
de la defensa antiestrés intracelular. Existe otro regulón, el OxyR, que es
independiente de SoxRX y responde al H2O2, dando cuenta
del otro 50 % de la defensa antioxidante, desencadenada por estrés oxidativo.
Algunos metales, tales como el
Se y el Zn, por su participación como cofactores de enzimas antioxidantes (GPx
y SOD citoplasmática, respectivamente), contribuyen a aumentar las defensas
antioxidantes.
La
catalasa se encuentra en todos los órganos, pero especialmente en el hígado y
en los eritrocitos. Localizada principalmente en peroxisomas, es una hemo proteína,
que tiene asociada una molécula de NADPH para estabilizar la molécula.
Rol
del glutation en la respuesta antioxidante
La GSH peroxidasa (GPx,
presente en mitocondrias, citosol y peroxisomas) contribuye a las defensas
antioxidantes, actuando en la regeneración del glutation a su estado reducido.
La tiorredoxina reductasa y algunas proteínas, tales como las metalotioneina,
ricas en residuos cisteínas, también participan en la restauración de los
niveles de GSH reducido, poseyendo por ello propiedades antioxidantes (26).
La melatonina (el principal
producto de la glándula pineal) es un atrapante de radicales libres (.OH,
NO. , 1O2
y
ONOO-), penetra distintas barreras intracelulares, se acumula en los
núcleos, donde protege al ADN de
distintos factores de estrés (efecto de metales, radiaciones ionizantes, etc.).
Entre los distintos tratamientos que se están aplicando para aminorar o
revertir los daños provocados por el estrés oxidativo, el uso de melatonina
parece muy promisorio. Wenbo y col. (27) probaron los efectos de melatonina,
manitol y trolox (atrapante de radicales libres) para inhibir la formación de
8OH Gu (indicador de daño al ADN), en un sistema experimental de daño por el
ácido d-aminolevúlico (dALA),
en presencia de hierro. Sus resultados indican que:
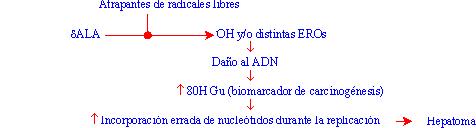
Entre las defensas
antioxidantes no enzimáticas, tiene un lugar predominante el glutation (GSH).
Esta pequeña molécula protege a la célula contra diferentes especies
oxidantes y se ha comprobado su participación clave en numerosos desórdenes
neurodegenerativos (28). Tanto el GSH como
otras moléculas conteniendo tioles, tienen alto poder reductor y, por
consiguiente, poseen propiedades antioxidantes, ya que pueden cederle un electrón
a las EROs y/o ERNs, disminuyendo de esta forma su reactividad. Se dice que este
tipo de compuestos de bajo peso molecular actúan como “atrapantes” de
radicales libres. Entre ellos podemos citar a la tiorredoxina (Trx) y a la
vitamina C o ácido ascórbico (hidrosoluble) y a las vitaminas liposolubles E o
alfa tocoferol (unida a membrana) y A o axeroftol.
Antioxidantes
en la alimentacion
La vitamina E captura
especialmente al radical oxidrilo, siendo su principal fuente el germen de
trigo; la vitamina A está presente en el aceite de hígado de pescado, en
vegetales (tales como la zanahoria) ricos en carotenoides y la vitamina C en cítricos,
tomate, frutilla y verduras. Las dos primeras, por ser liposolubles, pueden
acumularse en grasas y/o membranas y aun no se sabe qué consecuencia puede
tener el uso abusivo de las mismas, por eso es más aconsejable ingerirlas en
los productos naturales que en su forma aislada.
Estudios epidemiológicos
indican que la ingestión de frutas y vegetales confiere protección contra el
desarrollo de cáncer, frecuentemente asociado a estrés oxidativo. Si bien se
ha propuesto que el efecto benéfico de este tipo de alimentos radica en las
propiedades antioxidantes de las vitaminas (29, 30) que contienen, cuando se
administran vitaminas C y E y carotenoides puros no se obtienen resultados tan
concluyentes. A partir de este estudio Potter (30) concluye que frutas y
vegetales actuarían como una “polifarmacia” contra el desarrollo de
enfermedades crónicas, conteniendo no sólo vitaminas sino también otros
agentes antioxidantes, tales como los polifenoles (con propiedades de atrapantes
de radicales libres y quelantes de metales), formando una compleja trama
antioxidante. Los flavonoides son polifenoles antioxidantes, presentes en
plantas y posiblemente los beneficios de la ingestión de frutas, vegetales y
vino tinto, pregonado por los nutricionistas, radique en su alto contenido en
estos antioxidantes polifenólicos. Los polioles (ej: sorbol) también activan
fuertemente los caminos de señales sensibles a estrés (31).
Otros
mecanismos de protección
Además de los
mecanismos de protección antioxidante, enzimáticos y no enzimáticos, también
contribuyen a paliar el posible daño oxidativo:
1-
La fidelidad de las relaciones metabólicas de oxido reducción. Recordar
que, en el sitio IV de la cadena respiratoria, la presencia de los citocromos
a-a3 provee 4 sitios de
transferencia de electrones para hacer más efectiva la transferencia y
justamente allí no hay formación de EROs. En tanto que en los otros sitios a
lo sumo hay una pérdida del 4%, debido a que la suma de los potenciales de los
distintos sistemas de reducción intervinientes es francamente positivo, tirando
el equilibrio hacia la derecha (sitio I → sitio III→ sitio IV)
2-
Gran compartimentalización celular, lo que trae como consecuencia que
las EROs y sus fuentes no siempre estén cerca de sus blancos de acción.
3-
Varios factores estructurales de los ácidos nucleicos favorecen su
protección ante el estrés oxidativo: la cromatina compacta, la presencia de
histonas, la formación de complejos.
Destino celular
Cuando las
especies reactivas oxidantes superan las defensas antioxidantes se produce el
estrés oxidativo, hay daño a macromoléculas. La siguiente tabla resume los
principales daños.
|
ADN
Azúcar: base
propenal→ MDA
Bases: 8-Oxo Gu,
timina glicol y productos de hidrólisis espontánea
Azúcar + base:
5’,8- ciclo deoxiGu
Formación de
aductos entre radicales: ADN- ADN, ADN- proteína
|
PROTEINAS
Oxidación grupos
SH
Oxidación residuos
aromáticos
Ataque a la unión
peptídica → derivados carbonílicos→ clivaje
|
LIPIDOS
Iniciación,
propagación y terminación.
Formación de
radical lipídico (L.
). hidroperóxidos (LOO.), aductos con lípidos, ADN,
proteínas.
|
El posible
destino celular bajo condiciones de estrés, dependerá de varios factores: el
contenido endógeno de defensas antioxidantes, el grado de estimulación de las
mismas bajo la condición de estrés, la reversibilidad de las modificaciones a
macromoléculas producidas, la magnitud del estrés oxidativo y sus
consecuencias funcionales. Existen varios sistemas de reparación de daño al
ADN, y a nivel de proteínas hay muchas reacciones que son reversibles, en tanto
que los lípidos quizás sean las macromoléculas más establemente afectadas y
con consecuencias más directas sobre la integridad celular, de allí la gran
atención que se ha puesto en ellos.
Glosario
EROs:
especies reactivas del Oxígeno
ERNs:
especies reactivas del Nitrógeno
GSH:
glutation reducido
GSSG:
glutation oxidado
Trx:
tiorredoxina
O2-.: radical superóxido
HO.:
radical oxidrilo
Eº: potencial de reducción estándar
OCl-: hipoclorito
1O2: Oxígeno
singulete
8 oxo-Gu: 7-hidro-8-oxo
deoxignanosina
UVA: radiación ultravioleta A
MMP: metaloproteasas de matriz
ONOO-.: peroxinitrito
BLUE: especies bioluminiscentes
SOD: superóxido dismutasa
GPx: glutation peroxidasa





No hay comentarios:
Publicar un comentario